Veröffentlicht 1. Juli 2015 von Joe Dramiga
Harold E. Varmus: Chancen und Probleme der personalisierten Krebstherapie
Krebs ist weltweit die häufigste, krankheitsbedingte Todesursache und ziemlich komplex, denn den Krebs gibt es nicht: Unter dem Begriff werden viele, teilweise sehr unterschiedliche Krankheiten zusammengefasst. Es gibt etwa 200 verschiedene Krebsarten in den verschiedenen Körpergeweben, die wiederum bei jedem Patienten unterschiedlich ausgeprägt sein können. Daher wenden sich die Ärzte ab vom bisherigen „One-fits-all“-Prinzip der Krebstherapie hin zur stratifizierten Behandlung bestimmter Patienten-Subgruppen. Vielmehr noch möchten sie dem Patienten eine auf ihn zugeschnittene, persönliche Krebstherapie anbieten. Dafür brauchen sie eine molekularbiologische Diagnostik, die genetische Veränderungen im Tumor identifiziert und charakterisiert. Ihren Anfang nahm diese moderne Technologie in den späten Siebzigern des 20. Jahrhunderts mit den genetischen Experimenten von Varmus und Bishop.

Veränderte körpereigene Gene können Tumore auslösen
1970 glaubten viele Wissenschaftler, die Sarkomviren in Hühnern erforschten, dass diese Viren in Hühnern Sarkome verursachen, indem sie ihre Gene dauerhaft in das Genom der Zelle einschleusen. 1976 fanden Varmus und Bishop überraschenderweise heraus, dass diese Tumor auslösenden Virusgene zuerst den Hühnerzellen gestohlen wurden. Die Gene, die das Sarkom verursachen, sind zelleigene Gene, die einfach nur während des Diebstahls oder danach beschädigt wurden. Damit war nicht nur klar, dass Tumore eine genetische Ursache haben, sondern auch, wo man diese Krebsgene finden kann: im Genom von Tumor auslösenden Retroviren. Ein Befund, der sich für die zukünftige Krebsforschung als Glücksfall erwies: Denn die Genome von Retroviren enthalten nur vier bis elf Gene und sind mit sieben bis zwölf Kilobasenpaaren Länge sehr klein. Da die Virusgene bereits gut bekannt waren, war man in der Lage, diese Krebsgene dort sehr viel schneller zu entdecken als im menschlichen Genom mit seinen ca. 20.000 Genen und rund 3 Milliarden Basenpaaren. Recht bald fanden die Tumorforscher in Retroviren Krebsgene wie src (Rous sarcoma virus), abl (Abelson MLV), erbB (erythroblastosis ALV), kras (Ki-MLV), myc (MC29 myelocytoma ALV). Diesen Retroviren ist gemeinsam, dass sie meistens Sarkome oder Leukämien auslösen: Sie wurden daher (bis 1974) als RNA-Tumorviren bezeichnet.
Für ihre Arbeiten erhielten Varmus und Bishop 1989 den Nobelpreis für Physiologie und Medizin. Was damals eine revolutionäre Änderung des Blickwinkels auf das Syndrom Krebs war, ist heute Teil unseres medizinischen Allgemeinwissens: Krebsgene sind keine artfremden viralen Gene, sondern lebenswichtige körpereigene Gene, die wegen spezifischer Mutationen Amok laufen und eine gesunde Zelle in eine Tumorzelle verwandeln.
Spätere Arbeiten in der Zellkultur und in Mausmodellen zeigten, dass sich diese Verwandlung prinzipiell rückgängig machen lässt, wenn man die Transkription des Krebsgens dauerhaft blockiert oder es ganz entfernt. Erstmals gab es für Krebspatienten Hoffnung, dass Krebs prinzipiell heilbar ist, wenn man ihn ausreichend genetisch charakterisiert hat.

Die Proteine, die durch Krebsgene kodiert werden, haben spezifische zelluläre Funktionen
Die zellbiologische Analyse ergab, dass die Proteine, die durch retrovirale Krebsgene kodiert werden, die Zellteilung regulieren und eine der folgenden vier Funktionen haben:
1. Wachstumsfaktorrezeptoren
Ein Beispiel ist der epidermale Wachstumsfaktorrezeptor, der die Wundheilung fördert, indem er Zellwachstum auslöst. Als Beispiel dient hier das virale Krebsgen v-erbB in dem Avian Erythroblastosis Virus, das Hühner infiziert.
2. Proteinkinasen
Diese Proteine regulieren die Funktion von anderen Proteinen, indem sie diese an spezifischen Aminosäureresten phosphorylieren. Das virale Krebsgen v-src des Rous Sarcoma Virus, welches Hühner infiziert, ist hierfür ein Beispiel.
3. G-Proteine
G-Proteine binden an das Nukleotid GTP und besitzen eine GTPase-Aktivität, mit der sie eine Phosphatgruppe vom GTP abspalten können. Ein Beispiel hierfür ist das virale Krebsgen v-H-ras des Harvey Murine Sarcoma Virus, welches Ratten infiziert.
4. Transkriptionsfaktoren
Diese Proteine binden an DNA und aktivieren die Transkription. Das virale Krebsgen v-jun des Avian Sarcoma Virus, welches Hühner infiziert, ist hierfür ein Beispiel.
Die genetische Analyse von Tumoren durch Vollgenomsequenzierung
Um die genetische Analyse zu erleichtern, hat sich das International Cancer Genome Consortium (ICGC) vorgenommen, 50 verschiedene Krebsarten vollständig zu sequenzieren. Hierfür sequenzieren die Forscher pro Tumorart das Genom von je 500 Gewebeproben aus erkrankten Organen und aus gesundem Gewebe. Bei einer Vollgenomanalyse werden alle drei Milliarden Basen des menschlichen Genoms sequenziert. Um eine korrekte Sequenz zu erhalten, wird das Erbgut im Schnitt etwa 30 Mal gelesen. Hierfür sind mithilfe der „Next Generation Sequencing“-Technologie nur ein bis zwei Tage nötig. Die genetische Signatur der Mutationen soll helfen, eine maßgeschneiderte Therapie zu entwickeln.
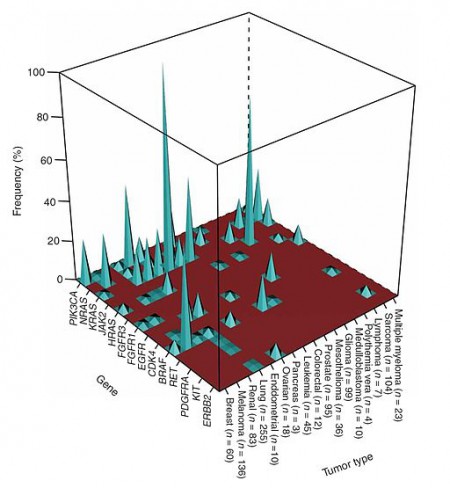
Bisher ist es allerdings nicht möglich, den Erfolg einer solchen Krebstherapie vorherzusagen. Forscher sequenzieren daher das Genom einzelner Krebspatienten sowie das Genom und Transkriptom (die Gesamtheit der transkribierten Gene) ihres Tumors als Basis für ein Computermodell eines virtuellen Patienten, um Wirkung und Nebenwirkungen von Therapien individuell vorhersagen zu können.
Ein Problem bereitet die Datenspeicherung, denn die produzierten Datenmengen sind enorm groß. Sie liegen im Bereich der Petabyte – das ist eine 1 mit 15 Nullen. Um diese Datenmengen verarbeiten zu können, wurde extra ein Datenanalyse-Zentrum aufgebaut. Auch die Interpretation der Daten ist nicht trivial. Nicht alle in Tumoren gefundenen Mutationen sind krebsrelevant, also sogenannte „driver mutations“. Bei vielen Mutationen handelt es sich um genetische Trittbrettfahrer, die in der Tumorevolution mitselektiert wurden („passenger mutations“). Darunter sind allerdings auch diejenigen Mutationen, die dem Tumor Medikamentenresistenz verleihen.
Man benötigt also viel diagnostische Fachkenntnis und geeignete Machine-Learning Algorithmen (MLA), um in der Menge der Mutationen die krebsrelevanten herauszufinden. Das verbesserte genetische Verständnis kann dazu führen, dass es zu einem Paradigmenwechsel in der Tumordiagnostik kommt: In Zukunft werden Tumore nicht mehr nach dem Ort ihrer Ausprägung im Gewebe, sondern nach dem ihnen zugrunde liegenden gestörten Signalweg klassifiziert. Eine Klassifikation, die sich nicht an den Symptomen, sondern an den Ursachen orientiert.
„Targeted Drugs“ werden vermutlich teurer als herkömmliche Krebsmedikamente
Wenn die Molekularbiologen den zugrunde liegenden gestörten Signalweg entdecken, können die Pharmazeuten beginnen, sogenannte „targeted drugs“ zu entwickeln. Welchen Nutzen solche Präparate bringen können, zeigt sich am Beispiel von Trastuzumab (Herceptin®). Zur Markteinführung wurde ein Überlebensgewinn von sechs Monaten diskutiert; heute ist klar, dass dieses Krebsmedikament das Leben von Brustkrebs-Patientinnen um mehr als ein Jahrzehnt verlängern kann. Trastuzumab wirkt aber nur bei Patienten mit einer spezifischen Mutation im Krebsgen. Ein Problem, das sich für die pharmazeutische Industrie damit stellt, ist, dass durch die Stratifizierung die Patientengruppen immer kleiner werden: Der Markt schrumpft. Der Trend geht zu mehr, aber kleineren Märkten. Da die Kosten für die Entwicklung eines solchen Medikaments aber gleich bleiben, müssen die Preise für solche Arzneimittel steigen, um die Forschungsausgaben wieder reinzuholen.
Damit diese Medikamente für alle Krebspatienten erschwinglich sind, müssen sich Krankenkassen, pharmazeutische Industrie und Gesundheitsministerien an einen Tisch setzen und in einer Public & Private-Partnership nach Lösungen für das Finanzierungsproblem suchen. Zusätzlich müssen die genomischen Daten der Krebspatienten geschützt werden, um genetische Diskriminierung durch Krankenversicherungen und Arbeitgeber zu verhindern.
Die personalisierte Krebstherapie setzt eine umfangreichere, genauere und damit teurere Diagnostik voraus, wird dafür aber einige Krebsarten heilen. Wie viel uns das wert ist, vor dem Hintergrund, dass Krebs weltweit pro Jahr ungefähr so viele Opfer fordert, wie Menschen in der Schweiz leben (8.2 Millionen), wird sich zeigen. Gesundheitsökonomen werden früher oder später eine Kosten-Nutzen-Analyse durchführen, mit deren weitreichenden ethischen und rechtlichen Implikationen wir uns alle beschäftigen müssen.